Como o tempo de disponibilidade de novos medicamentos varia na América Latina? Um novo relatório apresenta dados de 10 países da região: Argentina, Brasil, Chile, Colômbia, Costa Rica, República Dominicana, Equador, México, Panamá e Peru.
O FIFARMA Patient WAIT Survey, conduzido pela IQVIA, abrange 403 novas substâncias ativas em cinco áreas terapêuticas que foram aprovadas pelo FDA e/ou EMA no período 2014-2024. A disponibilidade denota o reembolso local – público ou privado – de medicamentos.
Para os dez países em análise, o tempo entre a primeira aprovação global e a autorização de introdução no mercado local foi em média de 38 meses. O tempo entre a autorização de comercialização local (no caso do Brasil, Anvisa) e a disponibilidade local (no caso do Brasil, após incorporação pela Conitec ao SUS) foi em média de 29 meses, o que significa que o tempo médio desde a primeira aprovação global até a disponibilidade local foi de 67 meses – mais de cinco anos e meio. O relatório não fornece dados sobre o atraso entre a primeira aprovação global e a apresentação de pedidos de autorização de comercialização pelas empresas em cada país da América Latina ou o tempo necessário para concluir cada processo regulatório nacional.
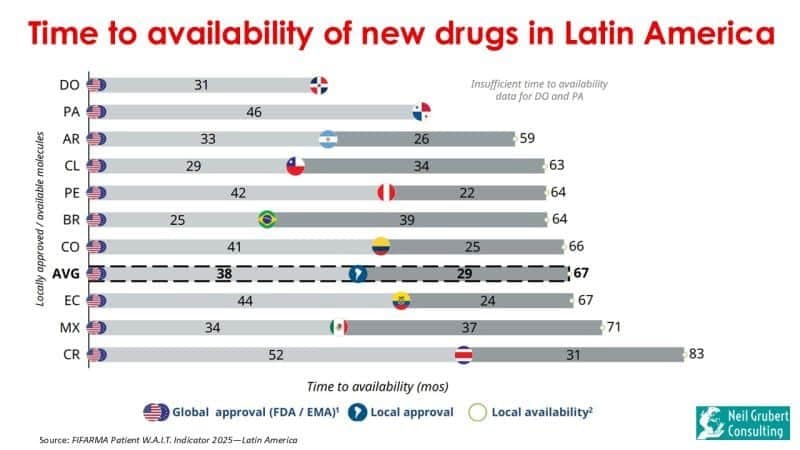
O Brasil é normalmente o primeiro país da região a concluir a autorização de comercialização – em média, 25 meses após a primeira aprovação global (pela Anvisa). No entanto, o país tem o tempo médio mais longo desde a aprovação regulatória até o reembolso – 39 meses – (Conitec) o que significa que o tempo médio desde a primeira aprovação global até a disponibilidade local é de 64 meses.
A Argentina tem o menor tempo médio desde a primeira aprovação global até a disponibilidade local: 59 meses. O prazo para a autorização de introdução no mercado local é de 33 meses, seguidos de 26 meses para a concessão do reembolso.
A Colômbia tem um atraso médio de disponibilidade de 66 meses: 41 meses para autorização de introdução no mercado local e 25 meses para reembolso.
No México, o tempo médio desde a primeira aprovação global até a disponibilidade local é de 71 meses: um atraso de 34 meses na obtenção da autorização de comercialização e 37 meses para negociar o reembolso.
A Costa Rica tem o maior atraso médio de disponibilidade na região (83 meses): 41 meses para autorização de comercialização local e 25 meses para reembolso.
Para obter informações sobre as diferenças nas taxas de disponibilidade de medicamentos mais novos na América Latina, clique aqui.


